蔡志强教授团队洪婷婷博士在Nanoscale Horizons及Microchimica Acta上分别发表毛细管电泳手性分离相关综述及研究论文
发布时间: 2023-09-05 访问次数: 630
近期,蔡志强教授团队在英国皇家化学会的纳米领域知名期刊Nanoscale Horizons(IF: 9.7)上发表题为“A cooperation tale of biomolecules and nanomaterials in nanoscale chiral sensing and separation”的综述文章,在分析化学领域知名期刊Microchimica Acta(IF: 5.7)上发表题为“Construction of chiral capillary electrochromatography microsystems based on Aspergillus sp. CM96”的研究论文。洪婷婷老师为论文的第一作者,蔡志强教授为论文通讯作者,常州大学为第一署名单位。
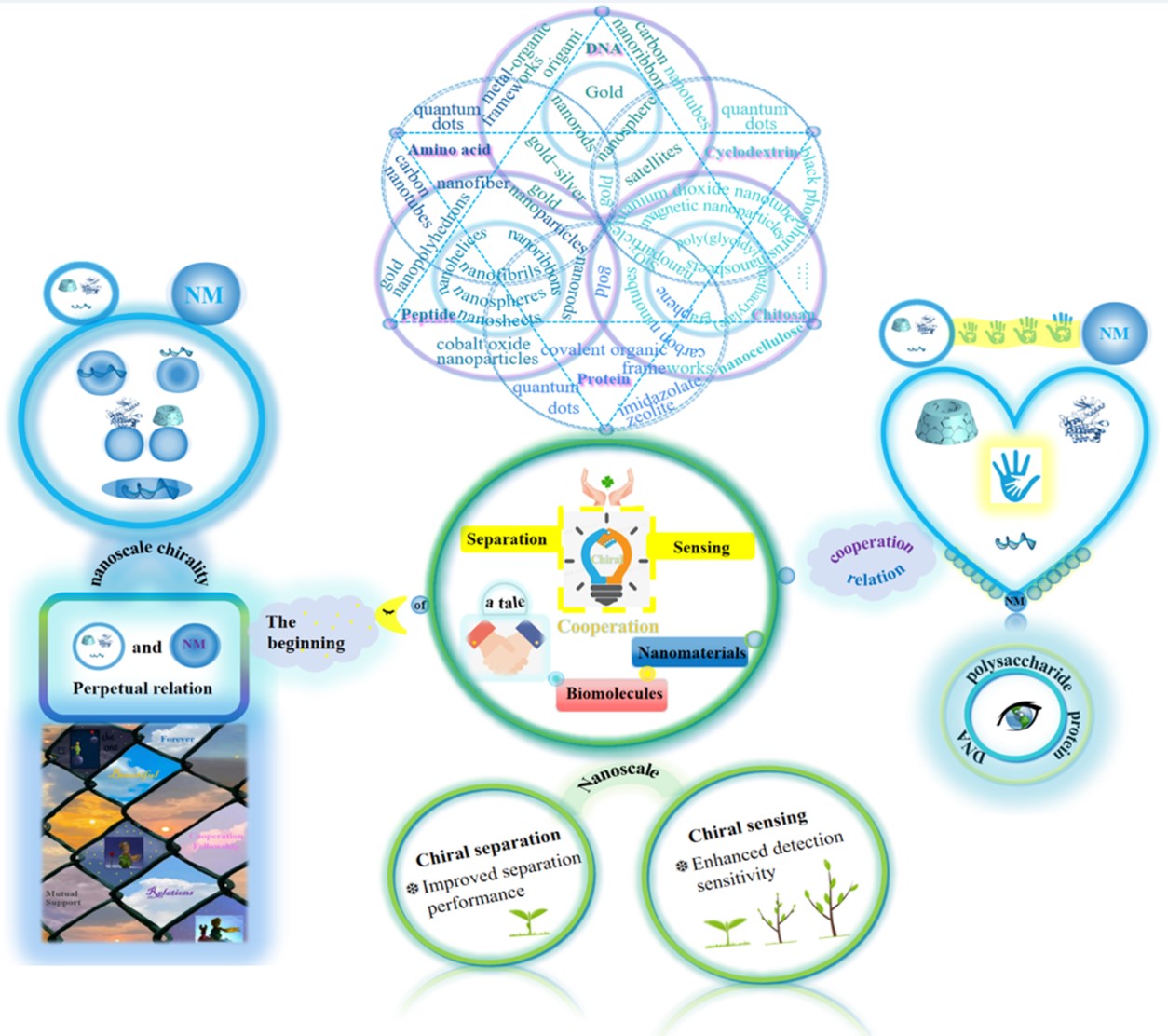
时空中各种美丽的关系交互组成一个多彩的世界。在一段合作的关系中,我们相互扶持,赋予彼此的价值以更丰富的内涵。本文分享了一个关于纳米尺度手性分离和传感领域中生物分子与纳米材料合作的故事。生物分子可作为构建手性分离系统和传感器的有效的手性供体,而纳米材料基于其特殊的理化性质可实现手性的传递和放大。我们主要综述了生物分子和纳米材料的结合在纳米尺度手性应用中的优势。近些年来,以提高传感器检测灵敏度为目标所建立的纳米材料和生物分子的新型合作方式引起了科研工作者的广泛关注。制备基于生物分子的新型纳米复合物在构建性能优越的手性分离体系领域也发挥着重要作用。本文详细描述了纳米材料与DNA,蛋白质,多肽,氨基酸,多糖等生物分子形成的关系网络。我们期待这个故事能够记录生物分子与纳米材料在纳米尺度手性应用中的永恒关系。
我们的研究工作围绕该综述的主题展开。我们选择了酶分子作为手性选择剂,采用基于氧化石墨烯纳米材料的固定化策略,将酶分子引入毛细管电色谱(CEC)手性分离体系。具有丰富官能团和较大比表面积的纳米材料是提高生物分子固定化效能的良好载体,纳米材料的引入可提高CEC手性分离效率和选择性。生物大分子在产生手性等离子体中起着至关重要的作用,“手性转移”可以通过将生物分子的手性传递给非手性纳米材料来实现,而较多研究报道空间维度上的手性传递。我们探索了时间维度的手性传递,并进一步从细胞水平探讨了CEC的手性分离性能。
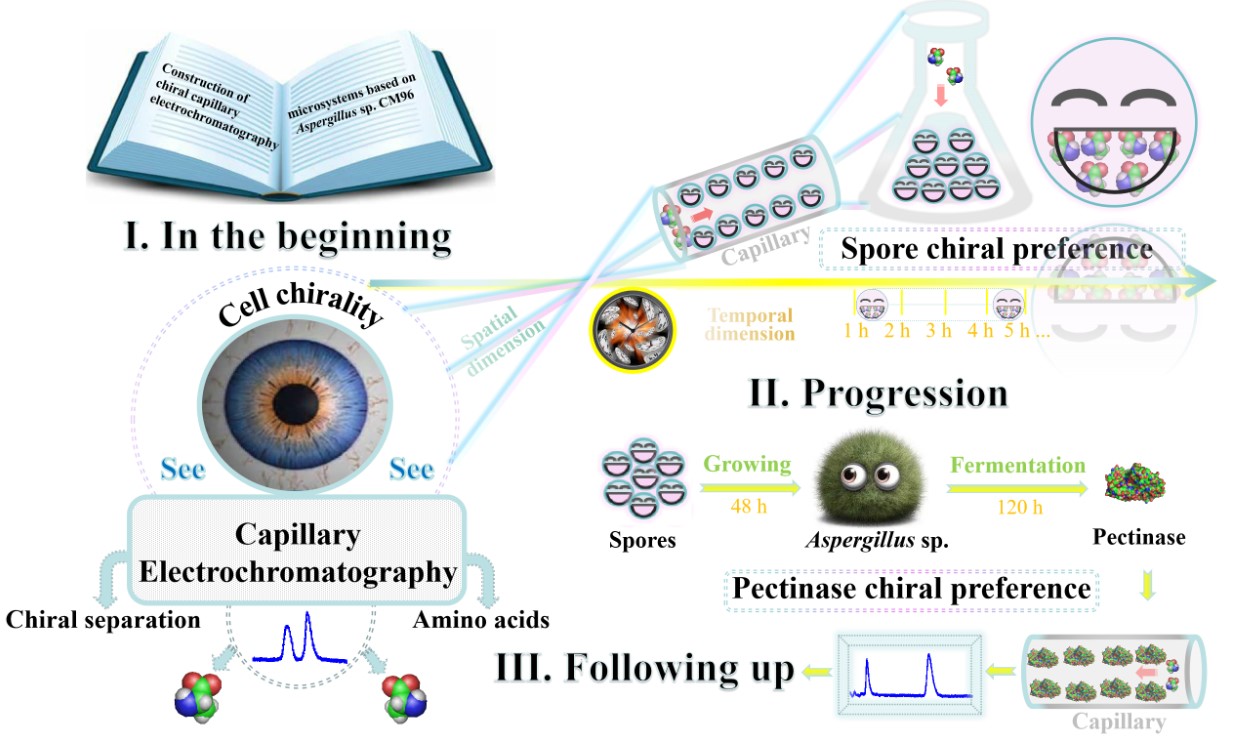
现今随着多学科交叉合作理念的深入,基于细胞的毛细管柱可为CEC微体系的构建注入新的活力,我们综述了将细胞引入毛细管柱的最新研究进展(Anal. Chem., 2022, 94, 1, 59-74)。细胞是由手性分子组成的,细胞水平的手性可受到细胞内蛋白质、氨基酸、多糖等分子手性的影响。其中,真核细胞骨架中的肌动蛋白和微管蛋白家族在细胞手性中起着重要作用。我们选用Aspergillus sp. CM96孢子(CM96s)初步构建了CEC手性分离体系。并已发现,具有褶皱结构的亚球状CM96s在细胞水平上具有手性分离能力。然而,毛细管柱有限空间中的手性分离仅反映CM96s-手性药物短暂的相互作用,我们从时空维度探索了CM96s的手性偏好。沿着CM96s生长的时间轨迹,我们见证了Aspergillus sp. CM96的生长和发酵过程。在发酵工程领域,Aspergillus sp.被广泛应用于生产各种酶类。酶类是内源性手性选择剂,其种类繁多,可规避其它手性选择剂需进行衍生化处理的繁琐反应步骤。构建手性药物与酶相互作用的微环境,更利于从分子水平上摸索酶的手性识别机理,酶分子作为CEC固定相在对映异构体分离中具有很大的应用前景。因此,我们也构建了基于Aspergillus sp. CM96产果胶酶-氧化石墨烯修饰的整体柱CEC体系,探索了CM96s在时间维度的手性传递。本研究以期为Aspergillus sp. CM96手性偏好的展示提供全新的CEC技术平台,有助于后期构建基于多种微生物的手性分离体系,记录其在手性CEC中的命运。
文章链接:
https://pubs.rsc.org/en/content/articlehtml/2023/nh/d3nh00133d
https://link.springer.com/article/10.1007/s00604-023-05926-5
https://pubs.acs.org/doi/10.1021/acs.analchem.1c04244

